Chương 3. AMIN, AMINO AXIT VÀ PROTEIN
Các hợp chất amin, amino axit, protein khá phổ biến trong tự nhiên và có nhiều ứng dụng trong đời sống và trong sản xuất. Nghiên cứu cấu trúc phân tử, mối quan hệ giữa cấu tạo và tính chất của các hợp chất sẽ giúp chúng ta hiểu được bản chất của các hợp chất chứa nitơ. Nội dung kiến thức của chương này bao gồm:
Bài 9: Amin
Bài 10: Amino axit.
Bài 11: Peptit và protein.
Chúng ta lần lượt xét từng bài học cụ thể của chương:
Bài 9: AMIN
A. BÀI GIẢNG
I. KHÁI NIỆM, PHÂN LOẠI VÀ DANH PHÁP
1. Khái niệm: Khi thay thế nguyên tử H trong phân tử $NH_{3}$ bằng gốc hiđrocacbon ta thu được amin.
Thí dụ:
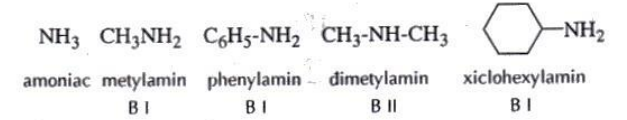
- Với các amin trên, ta thấy:
+ $CH_{3}NH_{2}$ và $C_{6}H_{5}NH_{2}$: có một nguyên tử H trong phân tử $NH_{3}$ được thay thế bằng gốc hiđrocacbon, ta nói các amin trên là amin bậc một.
+ $CH_{3}NHCH_{3}$: có hai nguyên tử H trong phân tử $NH_{3}$ được thay thế bằng gốc hiđrocacbon, ta nói các amin trên là amin bậc hai.
Vậy: Bậc của amin là số nguyên tử hiđro trong phân tử $NH_{3}$ bị thay thế bởi gốc hiđrocacbon.
- Amin thường có đồng phân về mạch cacbon, về vị trí nhóm chức và về bậc của amin
Thí dụ:
.png)
- CTPT đơn giản nhất của amin là $CH_{5}N$ nên các đồng đẳng của amin sẽ có dạng $CH_{5}(CH_{2})_{k}N$ hay $C_{k+1}H_{2k+5}N$. Đặt k + 1 = n thì $C_{n}H_{2n+3}N$ (n $\geq$ 1).
2. Phân loại
- Theo gốc hiđrocacbon có amin béo như $CH_{3}NH_{2}$, $C_{2}H_{5}NH_{2}$,..., amin thơm như $C_{6}H_{5}NH_{2}$, $CH_{3}C_{6}H_{4}NH_{2}$,...
- Theo bậc của amin có amin bậc I, amin bậc II, amin bậc III,...
3. Danh pháp: Gọi tên theo tên gốc chức (tên gốc hiđrocacbon + amin) và tên thay thế.
Thí dụ:
.png)
.png)
Như vậy, cách đọc tên như sau:
- Cách 1: (Tên gốc – chức): Tên amin = ank + yl + amin
- Cách 2: (Tên thay thế): Tên amin = ankan + vị trí + amin
II. TÍNH CHẤT VẬT LÍ
- Metylamin, đimetylamin, trimetylamin, etylamin là những chất khí, mùi khai, khó chịu, tan nhiều trong nước. Các amin có phân tử khối cao hơn là những chất lỏng hoặc rắn, độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
- Anilin là chất lỏng, không màu, ít tan trong nước và nặng hơn nước.
- Các amin đều rất độc. Thí dụ: Cây thuốc lá chứa amin (nicotin) rất độc.
III. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT HÓA HỌC
1. Cấu tạo phân tử
- Ta đã biết, tùy thuộc vào số liên kết và nguyên tử N tạo ra với nguyên tử cacbon mà ta có amin bậc I, bậc II, bậc III.
.png)
- Phân tử amin có nguyên tử nitơ tương tự trong phân tử $NH_{3}$ nên các amin có tính bazơ. Ngoài ra amin còn có tính chất của gốc hiđrocacbon.
2. Tính chất hóa học
a. Tính bazơ
- Tác dụng với nước: Dung dịch các amin mạch hở trong nước làm quỳ tím hóa xanh, phenolphtalein hóa hồng.
.png)
Anilin và các amin thơm phản ứng rất kém với nước.
- Tác dụng với axit
.png)
Nhận xét:
- Các amin tan nhiều trong nước như metylamin, etylamin,...có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein, có tính bazơ mạnh hơn amoniac nhờ ảnh hưởng của nhóm ankyl.
- Anilin có tính bazơ, nhưng dung dịch của nó không làm xanh giấy quỳ tím, cũng không làm hồng phenolphtalein vì tính bazơ của nó rất yếu và yếu hơn amoniac. Đó là ảnh hưởng của gốc phenyl (tương tự phenol).
Tính bazơ: $CH_{3}NH_{2}$ > $NH_{3}$ > $C_{6}H_{5}NH_{2}$
b. Phản ứng thế ở nhân thơm của anilin
.png)
Đây là phản ứng đặc trưng dùng để nhận biết anilin.
