§37. AXIT - BAZƠ – MUỐI
A. KIẾN THỨC CẦN NHỚ
1. Axit
a) Định nghĩa: Axit là hợp chất mà thành phần phân tử gồm có một hay nhiều nguyên tử hiđro liên kết với gốc axit, các nguyên tử hiđro này có thể thay thế bằng các nguyên tử kim loại.
b) Công thức hóa học: $H_{n}$(gốc axit)
(n = 1, 2, 3, ..; gốc axit: - Cl, = $SO_{4}$, - $NO_{3}$, $\equiv PO_{4}$,...)
c) Phân loại
- Axit không có oxi: HCl, $H_{2}S$,...
- Axit có oxi: $H_{2}SO_{4}$, $HNO_{3}$, $H_{3}PO_{4}$, $H_{2}SO_{3}$, ...
d) Tên gọi
- Axit không có oxi: Tên axit: axit + tên phi kim + hiđric
Ví dụ: HCl: axit clohiđric; $H_{2}S$: axit sunfuhiđric;...
- Axit có oxi:
+ Axit có nhiều nguyên tử oxi: Tên axit: axit + tên phi kim + ic
Ví dụ: $HNO_{3}$: axit nitric; $H_{2}SO_{4}$: axit sunfuric;...
+ Axit có ít nguyên tử oxi: Tên axit: axit + tên phi kim + ơ
Ví dụ: $H_{2}SO_{3}$: axit sunfurơ,...
2. Bazơ
a) Định nghĩa: Bazơ là hợp chất mà thành phần phân tử gồm có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều nhóm hiđroxit (-OH).
b) Công thức hóa học: $M(OH)_{n}$, n là hóa trị của kim loại
c) Tên gọi: Tên bazơ : tên kim loại (kèm hóa trị nếu kim loại có nhiều hóa trị) + hiđroxit
d) Phân loại
- Bazơ tan được trong nước: thường gọi là kiềm.
Ví dụ: NaOH, KOH, $Ca(OH)_{2}$, $Ba(OH)_{2}$...
- Bazơ không tan trong nước
Ví dụ: $Cu(OH)_{2}$, $Mg(OH)_{2}$, $Fe(OH)_{3}$,...
3. Muối
a) Định nghĩa: Muối là hợp chất mà thành phần phân tử gồm có một hay nhiều nguyên tử kim loại liên kết với một hay nhiều nhóm axit.
b) Công thức hóa học: $M_{m}$(gốc axit)$_{n}$
c)Tên gọi: Tên muối : tên kim loại (kèm hóa trị nếu kim loại có nhiều hóa trị) + tên gốc axit
d) Phân loại
- Muối trung hòa: Trong gốc axit không có nguyên tử hiđro H có thể thay thế bằng nguyên tử kim loại.
Ví dụ: $Na_{2}SO_{4}$, $CaCO_{3}$...
- Muối axit: Trong gốc axit còn có nguyên tử hiđro H chưa được thay thế bằng nguyên tử kim loại.
Ví dụ: $NaHSO_{4}$, $Ca(HCO_{3})_{2}$...
B. BÀI GIẢI CHI TIẾT CÁC CÂU HỎI VÀ BÀI TẬP
1. Bằng thí nghiệm hóa học, hãy chứng minh rằng trong thành phần của axit clohiđric có nguyên tố hiđro.
Trả lời:
Để xác định trong thành phần axit clohiđric có nguyên tố hiđro không người ta cho axit clohiđric tác dụng với kim loại (Fe, Zn, Al,...) thấy có khí hiđro bay ra.
2. Hãy viết công thức hóa học (CTHH) của những muối có tên sau: canxi clorua, kali nitrat, kali photphat, nhôm sunfat, sắt (III) nitrat.
Trả lời:
Công thức hóa học của những muối:
- Canxi clorua: canxi có hóa trị II, gốc axit có hóa trị I:
1 x II = 2 x I → công thức hóa học $CaCl_{2}$
- Kali nitrat: kali có hóa trị I, gốc nitrat có hóa trị I:
1 x I = 1 x I → công thức hóa học $KNO_{3}$
- Kali photphat: kali có hóa trị I, gốc axit $PO_{4}$ có hóa trị III:
3 x I = 1 x III → công thức hóa học $K_{3}PO_{4}$
- Nhôm sunfat: nhôm có hóa trị III, gốc axit $SO_{4}$ có hóa trị II:
2 x III = 3 x II → công thức hóa học $Al_{2}(SO_{4})_{3}$
- Sắt (III) nitrat: sắt có hóa trị III, gốc axit $NO_{3}$ có hóa trị I:
1 x III = 3 x I → công thức hóa học $Fe(NO_{3})_{3}$
3. Những hợp chất có công thức hóa học: KOH, $CuCl_{2}$, $Al_{2}O_{3}$, $ZnSO_{4}$, CuO, $Zn(OH)_{2}$, $H_{3}PO_{4}$, $CuSO_{4}$, $HNO_{3}$. Hãy cho biết mỗi hợp chất trên thuộc loại hợp chất nào?
Trả lời:
Những công thức hóa học trên thuộc loại hợp chất sau:
- Oxit bazơ : $Al_{2}O_{3}$, CuO;
- Axit: $H_{3}PO_{4}$, $HNO_{3}$;
- Bazơ: KOH, $Zn(OH)_{2}$;
- Muối : $ZnSO_{4}$, $CuCl_{2}$, $CuSO_{4}$.
4. Cho biết gốc axit và tính hóa trị của gốc axit trong các axit sau: $H_{2}S$, $HNO_{3}$, $H_{2}SO_{4}$, $H_{2}SiO_{3}$, $H_{3}PO_{4}$.
Trả lời:
- $H_{2}S$: gốc axit là S có hóa trị II.
- $HNO_{3}$: gốc axit là $NO_{3}$ có hóa trị I.
- $H_{2}SO_{4}$: gốc axit là $SO_{4}$ có hóa trị II.
- $H_{2}SiO_{3}$: gốc axit là $SiO_{3}$ có hóa trị II.
- $H_{3}PO_{4}$: gốc axit là $PO_{4}$ có hóa trị III.
5. Viết công thức của các hiđroxit ứng với các kim loại sau: Natri, canxi, crom, bari, kali, đồng, kẽm, sắt. Cho biết hóa trị của crom là III, đồng là II và sắt là III.
Trả lời:
Công thức các hiđroxit tương ứng là: NaOH, $Ca(OH)_{2}$, $Cr(OH)_{3}$, $Ba(OH)_{2}$, KOH, $Cu(OH)_{2}$, $Zn(OH)_{2}$, $Fe(OH)_{3}$.
6.Viết phương trình hóa học biểu diễn những biến hóa sau:
a) Ca → CaO → $Ca(OH)_{2}$
b) Ca → $Ca(OH)_{2}$
Trả lời:
Các phương trình hóa học biểu diễn những biến hóa:
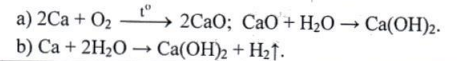
7. Hãy dẫn ra một phương trình hóa học đối với mỗi loại phản ứng sau và cho biết phản ứng hóa học thuộc loại nào?
a) Oxi hóa một đơn chất bằng oxi;
b) Khử oxit kim loại bằng hiđro ;
c) Đẩy hiđro trong axit bằng kim loại;
d) Phản ứng giữa oxit bazơ với nước;
e) Phản ứng giữa oxit axit với nước;
Trả lời:
a) Oxi hóa đơn chất bằng oxi thuộc loại phản ứng oxi hóa – khử.
Ví dụ: .png)
b) Khử oxit kim loại bằng hiđro, thuộc loại phản ứng oxi hóa – khử.
Ví dụ: .png)
c) Đẩy hiđro trong axit bằng kim loại thuộc loại phản ứng thế.
Ví dụ: .png)
d) Phản ứng giữa oxit bazơ với nước thuộc loại phản ứng hóa hợp.
Ví dụ: .png)
e) Phản ứng giữa oxit axit với nước thuộc loại phản ứng hóa hợp.
Ví dụ: .png)
8. Tính lượng natri hiđroxit thu được khi cho natri tác dụng với nước:
a) 46g natri ;
b) 0,3mol natri.
Trả lời:
a)Phương trình phản ứng là:
.png)
- Số mol Na là: $n_{Na}$ = $\large \frac{46}{23}$ = 2mol.
- Số mol NaOH thu được là: $n_{NaOH}$ = $n_{Na}$ = 2mol.
- Khối lượng NaOH thu được là: $m_{NaOH}$ = 2.40 = 80g.
b) Từ phương trình phản ứng hóa học trên ta thấy, cứ 2mol số mol Na luôn bằng số mol NaOH: $n_{NaOH}$ = $n_{Na}$ = 0,3mol. Khối lượng NaOH thu được là: $m_{NaOH}$ = 0,3.40 = 12g.
9. Trong các oxit sau đây, oxit nào tác dụng được với nước? Viết phương trình phản ứng và gọi tên sản phẩm tạo thành: $SO_{3}$ , CuO, $Na_{2}O$ , CaO , $CO_{2}$ , $Al_{2}O_{3}$.
Trả lời:
Những oxit tác dụng với nước: $SO_{3}$, $Na_{2}O$, CaO, $CO_{2}$.
- Oxit axit tác dụng với nước tạo axit tương ứng:
.png)
- Oxit bazơ tác dụng với nước tạo bazơ tương ứng:
.png)
10. Hãy trình bày những hiểu biết của em về axit clohiđric theo dàn ý sau:
a) Thành phần hóa học.
b) Tác dụng lên giấy quỳ.
c) Tác dụng với kim loại.
Trả lời:
a) Thành phần hóa học của axit clohiđric: công thức hóa học HCl, phân tử có 1 nguyên tử H, gốc axit là -Cl có hóa trị I.
b) Tác dụng với giấy quỳ: Dung dịch HCl làm đổi màu giấy quỳ tím thành đỏ.
c) Tác dụng với kim loại :
.png)
11.Trong những chất sau đây, những chất nào là oxit, bazơ, axit, muối: CaO, $H_{2}SO_{4}$, $Fe(OH)_{2}$, $FeSO_{4}$, $CaSO_{4}$, HCI, LiOH, $MnO_{2}$, $CuCl_{2}$, $Mn(OH)_{2}$, $SO_{2}$
Trả lời:
Trong những chất trên thì:
- Các chất là oxit: CaO, $MnO_{2}$, $SO_{2}$.
- Các chất là axit: $H_{2}SO_{4}$, HCl.
- Các chất là bazơ: $Fe(OH)_{2}$, LiOH, $Mn(OH)_{2}$.
- Các chất là muối: $FeSO_{4}$, $CaSO_{4}$, $CuCl_{2}$.
12. Viết phương trình hóa học biểu hiện những biến hóa sau đây:
.png)
Trả lời:
Các phương trình phản ứng hóa học biểu diễn những biến hóa trên:
.png)
13. Điền thêm những công thức hóa học của những chất cần thiết vào các phương trình phản ứng hóa học sau đây rồi cân bằng phương trình:
.png)
Trả lời:
Các phương trình hoàn chỉnh là:
.png)
14. Có thể điều chế được bao nhiêu mol axit sunfuric khi cho 240g lưu huỳnh trioxit $SO_{3}$ tác dụng với nước?
Trả lời:
Ta có $M_{SO_{3}}$ = 80 ; $n_{SO_{3}}$ = $\large \frac{240}{80}$ = 3mol.
- Phương trình phản ứng : .png)
- Từ phương trình trên ta thấy số mol $H_{2}SO_{4}$ tạo thành là: x = 3mol.
15. Viết công thức hóa học của các bazơ tương ứng với các oxit sau đây: CaO, FeO, $Li_{2}O$, BaO.
Trả lời:
Công thức hóa học của các bazơ tương ứng với các oxit trên là: CaO tương ứng với bazơ $Ca(OH)_{2}$, FeO tương ứng với bazơ $Fe(OH)_{2}$; $Li_{2}O$ tương ứng với bazơ LiOH; BaO tương ứng với bazơ $Ba(OH)_{2}$.
16. Viết công thức của các muối sau đây: a) kali clorua; b) canxi nitrat; c) đồng sunfat; d) natri sunfit; e) natri nitrat; f) canxi photphat; g) đồng cacbonat.
Trả lời:
Công thức của các muối có tên gọi trên là:
a) Kali clorua: KCl;
b) Canxi nitrat: $Ca(NO_{3})_{2}$;
c) Đồng sunfat: $CuSO_{4}$;
d) Natri sunfit: $Na_{2}SO_{3}$;
e) Natri nitrat: $NaNO_{3}$;
f ) Canxi photphat: $Ca_{3}(PO_{4})_{2}$;
g) Đồng cacbonat: $CuCO_{3}$.
17. Gọi tên các bazơ sau: $Ca(OH)_{2}$ , NaOH, KOH, $Al(OH)_{3}$ , $Mg(OH)_{2}$.
Trả lời:
Tên các bazơ: $Ca(OH)_{2}$: canxi hiđroxit; NaOH: natri hiđroxit (còn gọi là xút); KOH: kali hiđroxit (còn gọi là potat); $Al(OH)_{3}$: nhôm hiđroxit; $Mg(OH)_{2}$: magie hiđroxit.
18.Cho biết các chất dưới đây thuộc loại hợp chất nào, viết công thức của các hợp chất đó: Natri hiđroxit, khí cacbonic, khí sunfurơ, sắt (III) oxit, muối ăn, axit clohiđric, axit photphoric.
Trả lời:
Các chất trên thuộc loại các hợp chất sau:
- Oxit axit: khí cacbonic $CO_{2}$, khí sunfurơ $SO_{2}$.
- Oxit bazơ: Sắt (III) oxit $Fe_{2}O_{3}$.
- Bazơ: Natri hiđroxit NaOH.
- Axit: Axit clohiđric HCl, axit photphoric $H_{3}PO_{4}$.
- Muối: Muối ăn NaCl.
19. Tìm phương pháp xác định xem trong ba lọ, lọ nào đựng dung dịch axit, dung dịch muối ăn và dung dịch kiềm (bazơ).
Trả lời:
Cho giấy quỳ tím vào 3 mẫu thử đựng các dung dịch trên. Dung dịch nào làm quỳ tím thành màu đỏ là lọ đựng dung dịch axit; dung dịch nào làm quỳ tím chuyển màu xanh là lọ đựng dung dịch bazơ. Còn lại là lọ đựng dung dịch muối ăn, quỳ tím không đổi màu.
