Chương 4. OXI - KHÔNG KHÍ
§24. TÍNH CHẤT CỦA OXI
A. KIẾN THỨC CẦN NHỚ
- Kí hiệu hóa học: O; Công thức hóa học: $O_{2}$.
– Nguyên tử khối: 16; Phân tử khối: 32.
1. Tính chất vật lí
- Là chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
- Hóa lỏng ở – 183°C, khi hóa lỏng có màu xanh nhạt.
2. Tính chất hóa học
- Tác dụng với phi kim: Phi kim + oxi → oxit phi kim
Ví dụ:
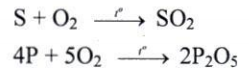
- Tác dụng với kim loại: Kim loại + oxi → oxit kim loại
Ví dụ:
.png)
- Tác dụng với hợp chất:
Ví dụ:
.png)
B. BÀI GIẢI CHI TIẾT CÁC CÂU HỎI VÀ BÀI TẬP
1.Oxi trong không khí là đơn chất hay hợp chất? Vì sao cá sống được trong nước? Những lĩnh vực hoạt động nào của con người cần thiết phải dùng bình nén oxi để hô hấp?
Trả lời:
Oxi trong không khí là đơn chất. Cá sống được trong nước vì có khí oxi hoà tan trong nước. Những lĩnh vực hoạt động của con người cần thiết phải dùng bình nén oxi để hô hấp là: thợ lặn, phi công vũ trụ, bệnh nhân khó thở, người làm việc ở các hầm mỏ sâu...
2. Trong ba bình giống hệt nhau và có chứa thể tích oxi như nhau. Đồng thời ta cho vào 3 bình: bình 1 một cục than đang cháy, bình 2 hai cục than đang cháy, bình 3 ba cục than đang cháy (các cục than có kích thước như nhau).
.png)
Em hãy nhận xét về hiện tượng xảy ra trong thí nghiệm trên?
Trả lời:
Vì ba bình có thể tích như nhau, bình 1 chỉ có 1 cục than, bình 2 có 2 cục than và bình 3 có 3 cục than nên cục than ở bình 1 cháy lâu hơn cục than cháy ở bình 2, cục than cháy ở bình 2 cháy lâu hơn cục than cháy ở bình 3 vì lượng oxi ở 3 bình như nhau.
3.Có những chất sau: $O_{2}$, Mg, P, Al, Fe.
Hãy chọn một trong những chất trên và hệ số thích hợp điền vào chỗ trống trong các phương trình hóa học sau:
.png)
Trả lời:
Các phương trình hoàn chỉnh là :
.png)
4. a) Cần bao nhiêu gam oxi để đốt cháy hoàn toàn 5mol cacbon? 5mol lưu huỳnh?
b) Trong giờ thực hành thí nghiệm, một em học sinh đốt cháy 3,2g lưu huỳnh trong 1,12 lít oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư?
Trả lời:
a) Phương trình phản ứng:
- Khi dùng oxi đốt cacbon:
.png)
- Khối lượng oxi để đốt cháy 5mol C là:
$m_{O_{2}}$ = 5.32 = 160g.
- Khi dùng oxi đốt lưu huỳnh:
.png)
- Khối lượng oxi để đốt cháy 5mol S là:
$m_{O_{2}}$ = 5.32 = 160g.
b) – Số mol lưu huỳnh:
$n_{S}$ = $\large \frac{3,2}{32}$ = 0,1mol
- Số mol oxi: $n_{O_{2}}$ = $\large \frac{1,12}{22,4}$ = 0,05mol
Từ phản ứng cháy của lưu huỳnh trong oxi ta thấy cứ 0,05mol oxi đốt cháy được 0,05mol lưu huỳnh. Do đó, số mol lưu huỳnh còn dư là: 0,1 - 0,05 = 0,05mol. Khối lượng lưu huỳnh còn dư là: $m_{S}$ = 0,05.32 = 1,6g.
5.Tính thể tích khí oxi và thể tích không khí (đktc) cần thiết để đốt cháy:
a) 1mol cacbon ;
b) 1,5mol photpho.
Cho biết oxi chiếm 20% thể tích không khí.
Trả lời:
a) Phương trình phản ứng đốt cháy cacbon:
.png)
- Thể tích oxi (đktc) cần dùng để đốt cháy 1mol C là:
$V_{O_{2}}$ = 1.22,4 = 22,4 lít.
- Thể tích không khí (đktc) cần dùng để đốt cháy 1mol C là:
$V_{kk}$ = $\large \frac{22,4}{20}$.100 = 112 lít
b) Phương trình phản ứng đốt cháy photpho:
.png)
- Số mol $O_{2}$ cần dùng là: x = $\large \frac{5.1,5}{4}$ = 1,875mol
- Thể tích oxi (đktc) cần dùng để đốt cháy 1,5 mol P là:
$V_{O_{2}}$ = 1,875.22,4 = 42 lít
- Thể tích không khí (đktc) cần dùng để đốt cháy 1,5 mol P là:
$V_{kk}$ = $\large \frac{42}{20}$.100 = 210 lít.
6. Cho một luồng không khí khô đi qua bột đồng (dư) nung nóng. Khí thu được sau phản ứng là:
a) cacbon đioxit; b)nitơ ;
c) oxi; d) hơi nước.
Tìm câu trả lời đúng.
Trả lời:
Khi cho một luồng không khí khô đi qua bột đồng (dư) nung nóng, khí thu được sau phản ứng là nitơ. Do đó, câu trả lời đúng là b.
7. Đốt cháy 1kg than trong khí oxi, biết than có 5% tạp chất không cháy.
a) Tính thể tích oxi (đktc) cần thiết để đốt cháy 1kg than trên.
b) Tính thể tích khí cacbonic (đktc) sinh ra trong phản ứng.
Trả lời:
- Khối lượng than nguyên chất: $m_{C}$ = $\large \frac{1000.95}{100}$ = 950g
- Số mol than nguyên chất : $n_{C}$ = $\large \frac{950}{12}$ = 79,167mol
- Phản ứng đốt cháy than trong oxi là:
.png)
a) Thể tích oxi (đktc) cần dùng để đốt cháy 1kg than là:
$V_{O_{2}}$ = 79,167.22,4 = 1773,3 lít.
b) Thể tích khí $CO_{2}$ (đktc) sinh ra bằng thể tích khí oxi tham gia là 1773,3 lít.
8. a) Trong 16 g khí oxi có bao nhiêu mol nguyên tử oxi và bao nhiêu mol phân tử oxi.
b)Tính tỉ khối của oxi với nitơ, với không khí.
Trả lời:
a) Trong 16g oxi có 1mol nguyên tử oxi và 0,5mol phân tử oxi ($\frac{16}{32}$ = 0,5).
b)- Tỉ khối của oxi với nitơ: $d_{O_{2}/N_{2}}$ = $\frac{M_{O_{2}}}{M_{N_{2}}}$ = $\frac{32}{28}$ $\approx$ 1,14.
- Tỉ khối của oxi với không khí: $d_{O_{2}/kk}$ = $\frac{M_{O_{2}}}{29}$ = $\frac{32}{29}$ $\approx$ 1,10.
