§11. TỔNG KẾT - LUYỆN TẬP
1. a) Hãy chỉ ra từ nào (những từ in đậm) chỉ vật thể tự nhiên, từ nào chỉ vật thể nhân tạo, từ nào chỉ chất trong các câu sau đây:
- Chậu có thể làm bằng nhôm hay chất dẻo.
- Xenlulozơ là thành phần chính tạo nên màng tế bào thực vật, có nhiều trong thân cây (gỗ, tre, nứa...)
b) Biết rằng sắt có thể bị nam châm hút, có khối lượng riêng D = 7,8g/$cm^{3}$; nhôm có D = 2,7g/$cm^{3}$ và gỗ tốt (coi như là xenlulozơ) có D = 0,8g/$cm^{3}$. Hãy nói cách làm để tách riêng mỗi chất trong hỗn hợp vụn rất nhỏ 3 chất.
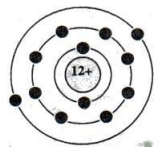
2. Cho biết hình dưới là sơ đồ nguyên tử magie.
a) Hãy chỉ ra: số p trong hạt nhân, số e trong nguyên tử, số lớp electron và số electron lớp ngoài cùng.
b) Nêu điểm khác nhau và giống nhau giữa nguyên tử magie và nguyên tử canxi (xem sơ đồ nguyên tử ở bài tập 5 bài 4 Nguyên tử, trang 16).
3. Một hợp chất có phân tử gồm 2 nguyên tử nguyên tố X liên kết với 1 nguyên tử O và nặng hơn phân tử hiđro 31 lần.
a) Tính phân tử khối của hợp chất.
b) Tính nguyên tử khối của X, cho biết tên và kí hiệu của nguyên tố (xem bảng 1 trang 42).
4. Điền các từ hay cụm từ thích hợp vào chỗ trống:
a) Những chất tạo nên từ hai ... trở lên được gọi là ...
b) Những chất có... gồm những nguyên tử cùng loại ... được gọi là ...
c)... là những chất tạo nên từ một ...
d) ... là những chất có ... gồm những nguyên tử khác loại...
e) Hầu hết các ... có phân tử là hạt hợp thành, còn ... là hạt hợp thành của ... kim loại.
5. Khẳng định sau gồm hai ý: “Nước cất là một hợp chất, vì nước cất sôi ở đúng 100°C”.
Hãy chọn phương án đúng trong số các phương án sau:
A. Ý 1 đúng, ý 2 sai.
B. Ý 1 sai, ý 2 đúng.
C. Cả hai ý đều đúng và ý 2 giải thích cho ý 1.
D. Cả 2 ý đều đúng nhưng ý 2 không giải thích cho ý 1.
E. Cả hai ý đều sai.
6. Cho biết sơ đồ nguyên tử một số nguyên tố như sau:
.png)
Hãy viết tên, kí hiệu hóa học và nguyên tử khối của mỗi nguyên tố.
7. Theo sơ đồ nguyên tử các nguyên tố cho trong bài tập 6, hãy chỉ ra:
a) Nguyên tử những nguyên tố nào có cùng số lớp electron (mấy lớp).
b) Nguyên tử những nguyên tố nào có cùng số electron lớp ngoài cùng (mấy electron).
8. a) Hãy tính xem trong 1g hiđro có bao nhiêu nguyên tử H (xem lại bài tập 7, thuộc bài học 5 : Nguyên tố hóa học, Hóa học 8 – NXB Giáo dục Việt Nam). Số nguyên tử H gần với con số nào nhất trong số các con số cho sau đây:
A. 4.$10^{23}$.
B. 5.$10^{23}$.
C. 6.$10^{23}$.
D. 5.$10^{23}$.
b) Trong 16g oxi có số nguyên tử O bằng hay lớn hơn số nguyên tử H trên.
9. Phân tử một hợp chất gồm nguyên tử nguyên tố X liên kết với 4 nguyên tử H và nặng bằng nguyên tử O
a. Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố X.
b. Tính phần trăm về khối lượng của nguyên tố X trong hợp chất.
10. Phân tử một hợp chất gồm nguyên tử nguyên tố Y liên kết với hai nguyên tử O. Nguyên tố oxi chiếm 50% về khối lượng của hợp chất.
a. Tính nguyên tử khối, cho biết tên và kí hiệu hóa học của nguyên tố Y.
b. Tính phân tử khối của hợp chất. Phân tử hợp chất nặng bằng nguyên tử nguyên tố nào?.
11. Dùng phễu chiết, hãy nói cách làm để tách nước ra khỏi dầu hỏa (dầu hôi).
Cho biết dầu hỏa là một chất lỏng có khối lượng riêng (D) khoảng 0,89g/ml và không tan trong nước.
12. Bảng dưới là khối lượng riêng của một số chất, ghi trong điều kiện thông thường.
Em có nhận xét gì về khối lượng riêng của các chất rắn so với các chất khí? Hãy giải thích vì sao?
.png)
13. Hãy tính hóa trị của đồng Cu, photpho P, silic Si và sắt Fe trong các công thức hóa học sau: $Cu(OH)_{2}$, $PCl_{5}$, $SiO_{2}$, $Fe(NO_{3})_{3}$.
14. Cho biết công thức hóa học hợp chất của nguyên tố X với O và hợp chất của nguyên tố Y với H như sau: (X,Y là những nguyên tố nào đó) XO, $YH_{3}$. Hãy chọn công thức hóa học nào là đúng cho hợp chất của X với Y trong số các công thức cho sau đây:
A. $XY_{3}$
B. $X_{3}Y$
C. $X_{2}Y_{3}$
D. $X_{3}Y_{2}$
E.XY.
15. Theo hóa trị của sắt trong hợp chất có công thức hóa học là $Fe_{2}O_{3}$, hãy chọn công thức hóa học đúng trong số các công thức hợp chất có phân tử gồm Fe liên kết với ($SO_{4}$) sau:
A. $FeSO_{4}$;
B. $Fe_{2}SO_{4}$
C. $Fe_{2}(SO_{4})_{2}$
D. $Fe_{2}(SO_{4})_{3}$
E. $Fe_{3}(SO_{4})_{2}$.
16. Lập công thức hóa học và tính phân tử khối của hợp chất có phân tử gồm kali K, bari Ba, nhôm Al lần lượt liên kết với:
a. Cl.
b. Nhóm ($SO_{4}$).
17. Viết sơ đồ công thức của các hợp chất sau: $H_{2}S$; $PH_{3}$; $CO_{2}$, $SO_{3}$.
18. Cho biết công thức hóa học hợp chất của nguyên tố X với nhóm ($SO_{4}$) và hợp chất của nhóm nguyên tử Y với H như sau: $X_{2}(SO_{4})_{3}$; $H_{3}Y$.
Hãy chọn công thức hóa học nào là đúng cho hợp chất của X và Y trong số các công thức cho sau đây:
(a). $XY_{2}$;
b). $Y_{2}X$;
(c). XY;
(d). $X_{2}Y_{2}$;
(e). $X_{3}Y_{2}$.
19. Lập công thức hóa học và tính phân tử khối của các hợp chất có phân tử gồm Na, Cu (II) và AI lần lượt liên kết với:
a) Brom Br (I).
b) Lưu huỳnh S (II).
20. Lập công thức hóa học và tính phân tử khối của các hợp chất có phân tử gồm Ag (I); Mg, Zn và Fe (III) lần lượt liên kết với:
a) Nhóm ($NO_{3}$).
b) Nhóm ($PO_{4}$)
21. Công thức hóa học một số hợp chất của nhôm viết như sau: $AlCl_{4}$; $AlNO_{3}$; $Al_{2}O_{3}$ ; AIS; $Al_{3}(SO_{4})_{2}$; $Al(OH)_{2}$, $Al_{2}(PO_{4})_{3}$.
Biết rằng trong số này chỉ có một công thức đúng và S có hóa trị II, hãy sửa lại những công thức sai.
HƯỚNG DẪN GIẢI VÀ TRẢ LỜI
1. a) Vật thể tự nhiên: thân cây (gỗ, tre, nứa); vật thể nhân tạo: chậu; chất: nhôm, chất dẻo, xenlulozơ.
b) Dùng nam châm hút sắt (tách riêng được sắt). Bỏ hỗn hợp còn lại vào nước, nhôm nặng hơn nên chìm xuống còn gỗ nổi lên. Gạn và lọc tách riêng được hai chất này.
2. a) Từ sơ đồ ta có: Số p trong hạt nhân là 12; số e trong nguyên tử là 12; số lớp electron là 3; số electron lớp ngoài cùng là 2.
b) Giữa magie và canxi có:
- Khác nhau: về số p và số e (ở nguyên tử magie là 12, ở canxi là 20); về số lớp electron (ở nguyên tử magie là 3, ở canxi là 4).
- Giống nhau: đều có 2 electron ở lớp ngoài cùng.
3. a) Vì hợp chất nặng hơn phân tử hiđro 31 lần nên phân tử khối của hợp chất bằng :
31.2 = 62 đvC
b) Vì hợp chất có phân tử gồm 2 X, 1 O nên phân tử khối bằng:
2X + 16 = 62
Suy ra: 2 X = 46 → X = 23 đvC.
X là natri (Na).
4. a) Những chất tạo nên từ hai nguyên tố hóa học trở lên được gọi là hợp chất.
b) Những chất có phân tử gồm những nguyên tử cùng loại liên kết với nhau được gọi là đơn chất.
c) Đơn chất là những chất tạo nên từ một nguyên tố hóa học.
d) Hợp chất là những chất có phân tử gồm những nguyên tử khác loại liên kết với nhau.
e) Hầu hết các chất có phân tử là hạt hợp thành, còn nguyên tử là hạt hợp thành của đơn chất kim loại.
5. Chọn D.
6. Từ sơ đồ nguyên tử ta biết được:
.png)
7. a) – Nguyên tử các nguyên tố liti, oxi và flo cùng có 2 lớp electron.
- Nguyên tử các nguyên tố natri, lưu huỳnh và clo cùng có 3 lớp electron.
b) – Nguyên tử các nguyên tố liti, natri và kali cùng có 1 electron ở lớp ngoài cùng. Nguyên tử các nguyên tố clo và flo cùng có 7 electron ở lớp ngoài cùng.
- Nguyên tử các nguyên tố lưu huỳnh và oxi đều có 6 e ở lớp ngoài cùng.
8. a) Khối lượng bằng gam của 1 nguyên tử H là: 1,66.$10^{-24}$g.
Suy ra, số nguyên tử H có trong 1 g hiđro bằng:
$\large \frac{1}{1,66.10^{-24}}$ = 6,02.$10^{23}$ nguyên tử
- Số nguyên tử H gần bằng với C.
b) Số nguyên tử O có trong 16g oxi bằng:
$\large \frac{16}{16.1,66.10^{-24}}$ = 6,02.$10^{23}$ nguyên tử.
Vậy: Số nguyên tử O bằng số nguyên tử H.
9. a) – Phân tử khối của hợp chất bằng nguyên tử khối của O = 16 đvC.
- Nguyên tử khối của nguyên tố X bằng: 16 – 4 = 12 đvC.
Vậy: X là nguyên tố cacbon C.
b) Phần trăm về khối lượng của một nguyên tố trong hợp chất bằng phần trăm về khối lượng của nguyên tố trong một phân tử.
Suy ra: Phần trăm về khối lượng của nguyên tố C trong hợp chất bằng:
%C = $\large \frac{12}{16}$.100% = 75%
10. a) Khối lượng bằng đơn vị cacbon của 2 nguyên tử oxi bằng: 2.16 = 32 đvC.
Vì mỗi nguyên tố chiếm 50% về khối lượng nên đây cũng là khối lượng của 1 nguyên tử nguyên tố Y. Suy ra nguyên tử khối của Y bằng 32 đvC, Y là lưu huỳnh S.
b) - Phân tử khối của hợp chất bằng: 32 + 2.16 = 64 đvC.
- Phân tử nặng bằng nguyên tử đồng (Cu = 64 đvC).
11. Cách chiết như sau: Đổ hỗn hợp nước và dầu hỏa vào phễu chiết. Dầu hỏa không tan trong nước và nhẹ hơn nước nên nổi thành một lớp ở trên. Nước tách thành một lớp ở dưới. Mở phễu cho nước chảy ra từ từ đến khi hết nước thì đóng khóa phễu lại.
12. Khối lượng riêng của các chất rắn lớn hơn rất nhiều (hàng nghìn lần) so với các chất khí là vì ở trạng thái khí các phân tử ở rất xa nhau, có khoảng trống rất lớn giữa các phân tử.
13.
- $Cu(OH)_{2}$: Vì nhóm OH hóa trị I nên: 1.a = 2.I → a = II: Cu hóa trị II.
- $PCl_{5}$: vì Cl hóa trị I nên 1.a = 5.I → a = V: P hóa trị V.
- $SiO_{2}$: vì O hóa trị II nên 1.a = 2.II → a = IV : Si hóa trị IV.
- $Fe(NO_{3})_{3}$: vì nhóm $NO_{3}$ hóa trị I nên 1.a = 3.I → a = III: Fe hóa trị III.
14.Chọn D. Theo công thức hóa học XO suy ra X hóa trị II; $YH_{3}$ suy ra Y hóa trị III.
- Công thức đúng là: $X_{3}Y_{2}$.
15.Chọn D. Theo công thức hóa học là $Fe_{2}O_{3}$, suy ra Fe có hóa trị III.
Công thức đúng là: $Fe_{2}(SO_{4})_{3}$
16. a) – Công thức hóa học KCl; phân tử khối là: 39 + 35,5 = 74,5.
- Công thức hóa học $BaCl_{2}$ ; phân tử khối 137 + 2.35,5 = 208.
- Công thức hóa học $AlCl_{3}$ ; phân tử khối 27 + 3.35,5 = 133,5.
b) - Công thức hóa học $K_{2}SO_{4}$ ; phân tử khối 2.39 + 32 + 4.16 = 174.
- Công thức hóa học $BaSO_{4}$ ; phân tử khối 137 + 32 + 4.16 = 233.
- Công thức hóa học $Al_{2}(SO_{4})_{3}$ ; phân tử khối 2.27 + 3.(32 + 4.16) = 342.
17. Sơ đồ công thức của các hợp chất sau: $H_{2}S$; $PH_{3}$; $CO_{2}$, $SO_{3}$.
- $H_{2}S$: H - S - H; $CO_{2}$: O = C = O;
.png)
18. Chọn C. Hóa trị của X theo công thức hóa học $X_{2}(SO_{4})_{3}$ là III.
Hóa trị của Y theo công thức hóa học $H_{3}Y$ là III.
Công thức đúng là XY.
19.a) - Công thức hóa học NaBr, phân tử khối bằng: 23 + 80 = 103 đvC.
- Công thức hóa học $CuBr_{2}$, phân tử khối bằng: 64 + 2.80 = 224 đvC.
- Công thức hóa học $AlBr_{3}$, phân tử khối bằng: 27 + 3.80 = 267 đvC.
b) - Công thức hóa học $Na_{2}S$, phân tử khối bằng: 2.23 + 32 = 78 đvC.
- Công thức hóa học CuS, phân tử khối bằng: 64 + 32 = 96 đvC.
- Công thức hóa học $Al_{2}S_{3}$, phân tử khối bằng: 2.27 + 3.32 = 150 đvC.
20. a) - Công thức hóa học $AgNO_{3}$, phân tử khối bằng:
108 + 14 + 3.16 = 170 đvC.
- Công thức hóa học $Mg(NO_{3})_{2}$, phân tử khối bằng:
24 + 2.(14 + 3.16) = 148 đvC.
- Công thức hóa học $Zn(NO_{3})_{2}$, phân tử khối bằng:
65 + 2.(14 + 3.16) = 189 đvC.
- Công thức hóa học $Fe(NO_{3})_{3}$, phân tử khối bằng:
56 + 3.(14 + 3.16) = 242 đvC.
b) - Công thức hóa học $Ag_{3}PO_{4}$, phân tử khối bằng:
3.108 + 31 + 4.16 = 419 đvC.
- Công thức hóa học $Mg_{3}(PO_{4})_{2}$, phân tử khối bằng:
3.24 + 2.(31 + 4.16) = 262 đvC.
- Công thức hóa học $Zn_{3}(PO_{4})_{2}$, phân tử khối bằng:
3.65 + 2.(31 + 4.16) = 385 đvC.
- Công thức hóa học $FePO_{4}$, phân tử khối bằng:
56 + 31 + 4.16 = 151 đvC.
21. - Vì Al hóa trị III nên công thức hóa học đúng: $Al_{2}O_{3}$.
- Sửa lại những công thức sai thành đúng: $AlCl_{3}$; $Al(NO_{3})_{3}$; $Al_{2}S_{3}$; $Al_{2}(SO_{4})_{3}$; $Al(OH)_{3}$; $AlPO_{4}$.
