151. Trong các phản ứng sau đây, ở phản ứng nào axit $H_{2}SO_{4}$ là axit đặc?
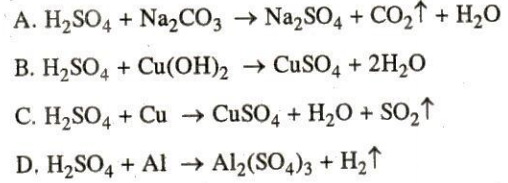
152. Một nguyên tố ở nhóm VIA có cấu hình electron nguyên tử ở trạng thái kích thích ứng với số oxi hoá +6 là
.png)
153. Hiđro peoxit tham gia các phản ứng hoá học :
.png)
Từ hai phản ứng trên nhận xét đúng là
A. Hiđro peoxit chỉ có tính oxi hoá.
B. Hiđro peoxit chỉ có tính khử.
C. Hiđro peoxit vừa có tính oxi hoá, vừa có tính khử.
D. Hiđro peoxit không có tính oxi hoá, không có tính khử.
154. Cho các hợp chất: $H_{2}O$, $Na_{2}O$, $F_{2}O$, $Cl_{2}O$.
Số hợp chất chứa oxi có số oxi hoá +2 là
A. 2.
B.1.
C. 3.
D. 4.
155. Khi cho ozon tác dụng lên giấy có tẩm dung dịch kali iotua và hồ tinh bột thấy xuất hiện màu xanh. Hiện tượng này xảy ra là do
A. sự oxi hoá ozon.
B. sự oxi hoá kali
C. sự oxi hoá iotua.
D. sự oxi hoá tinh bột.
156. Trong phương trình hoá học của phản ứng :
.png)
A. $H_{2}SO_{4}$ là chất oxi hoá, HI là chất khử.
B. HI bị oxi hoá thành $I_{2}$, $H_{2}SO_{4}$ bị khử thành $H_{2}S$.
C. HI oxi hoá $H_{2}SO_{4}$ thành $H_{2}S$ và nó bị khử thành $I_{2}$.
D. $H_{2}SO_{4}$ oxi hoá HI thành $I_{2}$ và nó bị khử thành $H_{2}S$.
Hãy chọn đáp án sai.
157. Cho axit sunfuric đặc phản ứng với các chất sau:
1. Đồng ; 2. Kim loại vàng; 3. Bazơ ; 4. Cacbon ; 5. Bari sunfat ; 6. Oxit lưỡng tính; 7. Bạc; 8. Hiđro clorua ; 9. Đường glucozơ; 10. Đồng sunfat.
Những phản ứng xảy ra được là
A. 1, 3, 6, 7, 9.
B. 2, 4, 6, 8, 10.
C. 1, 2, 4, 5, 7, 10.
D. 3, 5, 6, 8, 9, 10.
158. Độ bền của các liên kết hoá học theo dãy : $H_{2}O$, $H_{2}S$, $H_{2}Se$, $H_{2}Te$
A. tăng dần.
B. biến đổi không theo quy luật.
C. giảm dần.
D. không biến đổi.
159. Thể tích khí $SO_{2}$ (đktc) thu được khi đốt cháy hoàn toàn 12 gam pirit sắt là
A. 4,48 lít.
B. 2,64 lít.
C. 3,54 lít.
D. 8,12 lít.
160. Xác định khối lượng axit sunfuric thu được từ 1,6 tấn quặng chứa 60% $FeS_{2}$? Biết hiệu suất phản ứng là 100%.
A. 1568 kg.
B. 1,725 tấn.
C. 1,20 tấn.
D. 6320 kg.
161. Axit sunfuric và muối sunfat có thể nhận biết nhờ
A. chất chỉ thị màu.
B. dung dịch muối bari.
C. phản ứng trung hoà.
D. sợi dây đồng.
162. Trộn dung dịch chứa 1 mol axit $H_{2}SO_{4}$ với dung dịch chứa 1,5 mol NaOH. Sau khi phản ứng xảy ra hoàn toàn, cho dung dịch bay hơi đến khô.
Chất rắn thu được là
A. muối $NaHSO_{4}$.
B. hỗn hợp muối $NaHSO_{4}$ và $Na_{2}SO_{4}$.
C. muối $Na_{2}SO_{4}$.
D. hỗn hợp $NaHSO_{4}$, $Na_{2}SO_{4}$ và NaOH.
163. Trong phòng thí nghiệm người ta điều chế oxi bằng cách cho kali pemanganat tác dụng với hiđro peoxit theo sơ đồ phản ứng sau:
.png)
Thể tích $O_{2}$ (đktc) thu được khi dùng 2 mol $H_{2}O_{2}$ là
A. 44,8 lít.
B. 54,6 lít.
C. 32,4 lít.
D. 68,7 lít.
164. Khối lượng dung dịch axit $H_{2}SO_{4}$ 98% và khối lượng $H_{2}O$ cần dùng để pha chế 300 gam dung dịch $H_{2}SO_{4}$ 36% tương ứng là
A. 98 và 202 gam.
B. 60 và 240 gam.
C. 110,2 và 189,8 gam.
D. 92,5 và 207,5 gam.
165. Trong phản ứng hoá học :
.png)
Đã xảy га
A. sự khử $KMnO_{4}$.
B. sự khử $H_{2}O_{2}$.
C. sự oxi hoá $KMnO_{4}$.
D. sự oxi hoá axit $H_{2}SO_{4}$.
166. Các câu dưới đây, câu nào diễn tả không đúng tính chất của các chất ?
A. $O_{2}$ và $O_{3}$ đều có tính oxi hoá, nhưng $O_{3}$ có tính oxi hoá mạnh hơn.
B. $H_{2}O$ và $H_{2}O_{2}$ đều có tính oxi hoá, nhưng $H_{2}O_{2}$ có tính oxi hoá mạnh hơn.
C. Axit $H_{2}SO_{3}$ và axit $H_{2}SO_{4}$ đều có tính oxi hoá, nhưng axit $H_{2}SO_{4}$ có tính oxi hoá mạnh hơn.
D. $H_{2}S$ và $H_{2}SO_{4}$ đều có tính oxi hoá, nhưng $H_{2}SO_{4}$ có tính oxi hoá mạnh hơn.
167. Axit có những tính chất :
1. Phản ứng với một số muối.
2. Phản ứng với đồng.
3. Phản ứng với nhôm.
4. Phản ứng với tất cả các oxit.
5. Làm mất màu các thuốc thử.
6. Tạo thành muối axit.
Những ý đúng với axit sunfuric loãng là
A. 1, 3, 6.
B. 1, 2, 3, 5.
C. 2, 3, 5, 6.
D. 1, 2, 3, 4, 5.
168. Lưu huỳnh đioxit tham gia những phản ứng sau :
.png)
A. Ở phản ứng (1) $SO_{2}$ là chất khử, $Br_{2}$ là chất oxi hoá.
B. Ở phản ứng (2) $SO_{2}$ là chất oxi hoá, $H_{2}S$ là chất khử.
C. Ở phản ứng (2) $SO_{2}$ vừa là chất khử vừa là chất oxi hoá.
D. Ở phản ứng (1) $SO_{2}$ là chất khử, phản ứng (2) $H_{2}S$ là chất khử.
Hãy chọn đáp án sai.
169. Tính axit của dung dịch các oxit theo dãy :
.png)
A. giảm dần.
B. tăng dần.
C. không biến đổi.
D. không có những oxit này.
170. Nguyên tử của những nguyên tố nào ứng với cấu hình electron lớp ngoài cùng như sau :
.png)
A. Sb, N, As, P.
B. Bi, P, Sb, N.
C. As, P, N, Bi.
D. N, Sb, P, Bi.
171. Nitơ phản ứng trực tiếp với oxi ở nhiệt độ
A. 100°C.
B. 1000°C.
C. 300°C.
D. 3000°C.
172. Ở nhiệt độ thường, nitơ chỉ phản ứng được với
A. clo.
B. liti.
C. oxi.
D. đồng.
173. Tính chất đặc trưng của amoniac là :
1. Hòa tan tốt trong nước ; 2. Nặng hơn không khí ; 3. Tác dụng với kiếm. Phản ứng với : 4. Axit; 5. Muối ; 6. Oxi; 7. Khử hiđro.
Những tính chất nêu đúng :
A. 1, 2, 4, 5.
B. 2, 3, 4, 6.
C. 1, 2, 3, 4, 5, 6, 7.
D. 1, 4, 6.
174. Trộn 2 thể tích dung dịch axit $H_{2}SO_{4}$ 0,2M với 3 thể tích dung dịch axit $H_{2}SO_{4}$ 0,5M được dung dịch axit $H_{2}SO_{4}$ có nồng độ mol là
A 0,40M.
B. 0,25M.
C. 0,38M.
D. 0,15M.
175. Có ý kiến cho rằng tính chất đặc trưng của axit nitric là :
1. Bị phân hủy dưới tác dụng của ánh sáng.
2. Trên bề mặt axit khi bị đun nóng có thể cháy thành ngọn lửa.
3. Làm protein chuyển thành màu vàng.
4. Làm thoát ra $N_{2}O_{5}$ khi phản ứng với magie.
5. Làm thoát ra $NO_{2}$ khi phản ứng với đồng.
6. Phát sáng trong bóng tối.
Có bao nhiêu ý sai ?
A. 2.
B. 3.
C. 4.
D. 5.
176. Cho những hạt nhỏ của hai kim loại khác nhau vào hai ống nghiệm đựng axit $HNO_{3}$ đặc, nguội:
- Ở ống nghiệm thứ nhất thoát ra khí màu nâu.
- Ở ống nghiệm thứ hai không có phản ứng xảy ra.
Hai kim loại đã dùng tương ứng trong 2 thí nghiệm là
A. Zn và Ba.
B. Ag và Ca.
C. Cu và Al.
D. Na và Pb.
177. Dãy muối nitrat nào trong 4 dãy dưới đây khi bị đun nóng phân hủy tạo ra các sản phẩm gồm : oxit kim loại + $NO_{2}$ + $O_{2}$?
.png)
178. Dãy muối nitrat nào trong 4 dãy dưới đây khi bị đun nóng đều phân hủy tạo ra sản phẩm gồm : kim loại + $NO_{2}$ + $O_{2}$?
.png)
179. Quá trình sản xuất axit nitric trong công nghiệp được tiến hành qua một số công đoạn sau :
1. Oxi hóa NO; 2. Phản ứng của $NO_{2}$ với $H_{2}O$; 3. Oxi hóa $NH_{3}$; 4. Chuẩn bị hỗn hợp amoniac và không khí; 5. Tổng hợp $NH_{3}$.
Trật tự sắp xếp các công đoạn đúng là
A. 1, 3, 2, 4, 5.
B. 5, 4, 3, 1, 2.
C. 4, 5, 3, 1, 2,
D. 3, 4, 5, 1, 2.
180. Một học sinh nêu các tính chất hóa học của axit photphoric là :
1. Phân li trong dung dịch nước.
2. Làm phenolphatalein có màu hồng.
Tác dụng với :3. amoniac ;4. oxit bazơ; 5. đồng khi đun nóng ; 6. kẽm; 7, một số muối ; 8. axit nitric.
Những tính chất nêu sai là
A. 2, 4, 5, 8.
B. 1, 2, 4, 8.
C. 1, 2, 6, 7.
D. 2, 5, 8.
HƯỚNG DẪN TRẢ LỜI
151. Phản ứng C.
Hướng dẫn trả lời :
Axit $H_{2}SO_{4}$ đặc tham gia phản ứng thì số oxi hoá +6 của lưu huỳnh .png) luôn giảm xuống các số oxi hoá thấp hơn (+4, 0, -2).
luôn giảm xuống các số oxi hoá thấp hơn (+4, 0, -2).
Trong 4 phản ứng đã cho, chỉ có phản ứng C là số oxi hoá của .png) thay đổi (giảm xuống +4 ở $SO_{2}$). Do đó, axit $H_{2}SO_{4}$ tham gia phản ứng này là axit đặc.
thay đổi (giảm xuống +4 ở $SO_{2}$). Do đó, axit $H_{2}SO_{4}$ tham gia phản ứng này là axit đặc.
152. Cấu hình electron đúng là D.
Hướng dẫn trả lời :
Theo cấu hình này, nguyên tử ở trạng thái kích thích đã có 1 electron ở phân lớp 3s và 1 electron ở phân lớp 3p nhảy ra phân lớp 3d để lớp ngoài cùng của nguyên tử có 6 electron độc thân. Khi tham gia liên kết, nó đã dùng cả 6 electron độc thân này để có số oxi hoá +6.
153. Nhận xét đúng là C.
Hướng dẫn trả lời :
- Ở phản ứng (1), $H_{2}O_{2}$ thể hiện tính oxi hoá.
- Ở phản ứng (2), $H_{2}O_{2}$ thể hiện tính khử.
⇒ $H_{2}O_{2}$ vừa thể hiện tính oxi hoá vừa thể hiện tính khử.
154. Đáp án đúng là B.
Hướng dẫn trả lời :
- Chỉ có trong hợp chất $F_{2}O$ (thường viết là $OF_{2}$), oxi có số oxi hoá 2+.
155. Đáp án đúng là C.
156. Đáp án sai là C.
157. Đáp án đúng là A.
158. Đáp án đúng là C.
159. Đáp số đúng là A.
Hướng dẫn trả lời :
Phương trình phản ứng đốt quặng pirit để thu khí $SO_{2}$:
.png)
Số mol $FeS_{2}$: .png)
Theo phương trình phản ứng :
Số mol $SO_{2}$: $n_{SO_{2}}$ = 2$n_{FeS_{2}}$ = 0,1.2 = 0,2 (mol).
Vậy : $V_{SO_{2}}$ = 0,2.22,4 = 4,48 (lít).
160. Đáp số đúng là A.
Hướng dẫn trả lời :
Các phương trình phản ứng xảy ra trong quá trình sản xuất axit $H_{2}SO_{4}$ từ quặng pirit:
.png)
Ta có sơ đồ :
.png)
Khối lượng axit $H_{2}SO_{4}$ thu được là :
.png)
161. Đáp án đúng là B.
162. Đáp án đúng là B.
Hướng dẫn trả lời :
Khi cho axit $H_{2}SO_{4}$ tác dụng với NaOH:
Đầu tiên xảy ra phản ứng :
.png)
Sau phản ứng còn dư : 1,5 – 1 = 0,5 (mol) NaOH.
Tiếp tục xảy ra phản ứng:
.png)
Như vậy sau khi cô cạn trong hỗn hợp có 0,5 mol $NaHSO_{4}$ và 0,5 mol $Na_{2}SO_{4}$
163. Đáp số đúng là A.
Hướng dẫn trả lời :
Cân bằng phương trình phản ứng:
.png)
Theo phương trình phản ứng :
Số mol oxi thu được : $n_{O_{2}}$ = $n_{H_{2}O_{2}}$ = 2 mol.
⇒ Vậy : $V_{O_{2}}$ = 2 . 22,4 = 44,8 (lít).
164. Đáp số đúng là C.
Hướng dẫn trả lời :
Áp dụng quy tắc đường chéo (quy tắc trộn lẫn):
.png)
Vậy để có 300 gam dung dịch $H_{2}SO_{4}$ 36% cần lấy 110,2 gam dung dịch axit $H_{2}SO_{4}$ 98% pha với 189,8 gam $H_{2}O$.
165. Đáp án đúng là A.
166. Đáp án đúng là D.
Hướng dẫn trả lời :
Trong $H_{2}S$, lưu huỳnh có số oxi hoá –2, là số oxi hoá thấp nhất của lưu huỳnh, nên nó chỉ có tính khử, không có tính oxi hoá.
167. Đáp án đúng là A.
Hướng dẫn trả lời :
Axit $H_{2}SO_{4}$ loãng :
- Không phản ứng được với Cu.
- Không phản ứng được với một số oxit phi kim.
- Không làm mất màu các thuốc thử mà chỉ làm đổi mầu một số thuốc thử.
Do đó, các ý 2, 4, 5 sai. Các ý đúng là 1, 3 và 6.
168. Đáp án sai là C.
Ở phản ứng (2), $SO_{2}$ chỉ đóng vai trò chất oxi hóa.
169. Đáp án đúng là A.
170. Đáp án đúng là B.
Bi ở chu kì 6 ⇒ có 6 lớp electron ($6s^{2}6p^{3}$).
P ở chu kì 3 ⇒ có 3 lớp electron ($3s^{2}3p^{3}$).
Sb ở chu kì 5 ⇒ có 5 lớp electron ($5s^{2}5p^{3}$).
N ở chu kì 2 ⇒ có 2 lớp electron ($2s^{2}2p^{3}$).
171. Đáp án đúng là D.
172. Đáp án đúng là B.
173. Đáp án đúng là D.
174. Đáp án đúng là C.
Hướng dẫn trả lời :
Giả sử lấy 2 lít dung dịch axit $H_{2}SO_{4}$ 0,2M pha với 3 lít dung dịch $H_{2}SO_{4}$ 0,5 M :
2 lít dd $H_{2}SO_{4}$ 0,2M có 0,4 mol $H_{2}SO_{4}$
3 lít dd $H_{2}SO_{4}$ 0,5M có 1,5 mol $H_{2}SO_{4}$.
⇒ Số mol $H_{2}SO_{4}$ là 0,4 + 1,5 = 1,9 mol.
Thể tích dung dịch sau pha là 3 + 2 = 5 lít.
.png)
175. Đáp án đúng là A.
Hai tính chất nêu sai là 4 và 6.
176. Đáp án đúng là C.
Hướng dẫn trả lời :
.png)
Al bị thụ động hóa trong $HNO_{3}$ đặc nguội, nên không có phản ứng.
177. Đáp án đúng là A.
178. Đáp án đúng là B.
179. Đáp án đúng là B.
180. Đáp án đúng là D.
