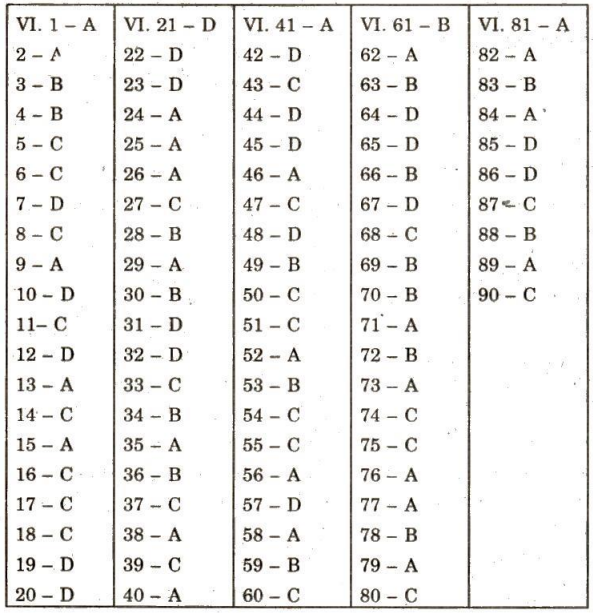
ĐÁP ÁN
VI.3. .png) = 0,1 mol
= 0,1 mol
Nếu chất rắn X chỉ có .png) và Fe thì
và Fe thì
.png) = 102.0,1 +0,2.56 = 21,4 g (< 24,1 g)
= 102.0,1 +0,2.56 = 21,4 g (< 24,1 g)
Suy ra trong X còn có Al dư 24,1 - 21,4 = 2,7 g
X + HCl → khí?
.png)
.png)
.png) = 0,35.22,4 = 7,84 lít
= 0,35.22,4 = 7,84 lít
VI.5. .png)
Vì phản ứng hoàn toàn mà hỗn hợp sau phản ứng tác dụng với NaOH sinh ra .png) , suy ra Al còn dư.
, suy ra Al còn dư.
Phần 1:
.png)
Chất rắn còn lại là Fe = .png) = 0,3 mol
= 0,3 mol
Phần 2: Có bao nhiêu mol Al? Fe?
Nếu đem phần 1 tác dụng với .png) thì sinh ra bao nhiêu mol NO?
thì sinh ra bao nhiêu mol NO?
.png)
Suy ra ở phần 2 (.png) = 1 mol) khối lượng của Al và Fe gấp đôi phần 1.
= 1 mol) khối lượng của Al và Fe gấp đôi phần 1.
Vậy: tổng số mol Fe tạo thành là 0,3 + 0,3.2 = 0,9 mol
Mol Al phản ứng = .png) .0,9 = 0,8 mol
.0,9 = 0,8 mol
Mol Al dư = 0,2 + 0,2.2 = 0,6 mol
Mol .png) =
= .png) = 0,3 mol
= 0,3 mol
Khối lượng hỗn hợp bột (Al + .png) ) ban đầu:
) ban đầu:
m = (0,8 + 0,6)27 + 0,3.232 = 107,4 gam
VI.22.
.png)
Chọn .png) để dùng thuốc thử.
để dùng thuốc thử.
VI.26. * Trong 100 ml dd Y:
.png) = 0,1.0,2 = 0,02 mol
= 0,1.0,2 = 0,02 mol
.png) = 0,1.0,3 = 0,03 mol
= 0,1.0,3 = 0,03 mol
→ .png) = 0,05 mol.
= 0,05 mol.
* Gọi V(lít) là thể tích dung dịch X cần:
.png) = V.0,2 mol → V.0,2 mol
= V.0,2 mol → V.0,2 mol .png)
.png) = V.0,1 mol → V.0,2 mol
= V.0,1 mol → V.0,2 mol .png)
→ .png) = 0,4. V mol.
= 0,4. V mol.
* Sau khi trộn lẫn thu được dd có pH = 7, suy ra phản ứng trung hòa vừa đủ.
.png)
* Ta có:
.png)
0,4.V = 0,05
V = 0,125 lít = 125 ml
VI.28. .png) = 1 mol
= 1 mol
.png)
Dung dịch thu được là dd KOH
.png) = 1.56 = 56 gam
= 1.56 = 56 gam
.png)
.png) = 39 + 362 - 0,5.2 = 400 gam
= 39 + 362 - 0,5.2 = 400 gam
C% = .png) .100% = 14%
.100% = 14%
VI.29. .png) = 0,1 mol;
= 0,1 mol; .png) = 0,1 mol
= 0,1 mol
.png)
Trong dd: .png) không bị thủy phân.
không bị thủy phân.
.png) bị thủy phân, tạo môi trường bazơ
bị thủy phân, tạo môi trường bazơ
.png)
VI.30. * Tính số mol NaOH?
dd NaOH có pH = 12 → pOH = 14 – 12 = 2
pOH = 2 → .png) = 0,01 M = [NaOH]
= 0,01 M = [NaOH]
.png) = 0,01.0,1 = 0,001 mol
= 0,01.0,1 = 0,001 mol
* Sau khi trung hòa, dung dịch thu được có
pH = 2 ⇒ .png) còn dư.
còn dư.
.png)
Tính số mol .png) còn dư?
còn dư?
pH = 2 → .png) = 0,01 M;
= 0,01 M; .png) = 0,01.0,2 = 0,002 mol
= 0,01.0,2 = 0,002 mol
.png)
* Tổng số mol .png) ban đầu:
ban đầu:
0,0005 + 0,002 = 0,0025 mol
.png)
VI.32.
.png)
.png)
Ta có:
.png)
VI.33.
.png)
Gọi số mol NaCl là a mol.
.png)
a = .png) = 0,002 mol
= 0,002 mol
.png) = 0,002.58,5 = 0,117 g
= 0,002.58,5 = 0,117 g
.png) = 2 – 0,117 = 1,883 g
= 2 – 0,117 = 1,883 g
%NaOH = .png) .100% = 94,15%
.100% = 94,15%
VI.34. * Tìm số mol .png) ?
?
Trong dung dịch A
.png)
Trong dung dịch B, x là nồng độ .png) .
.
.png)
Phản ứng giữa A và B vừa đủ tạo ra kết tủa theo sơ đồ:
.png)
Trong kết tủa thu được, tổng điện tích âm bằng tổng điện tích dương. Ta có:
0,01.2 + 0,01.2 = 0,005.2 + 0,1.2x
x = 0,15
.png) = 0,1x =0,015 mol
= 0,1x =0,015 mol
* Khối lượng kết tủa bằng tổng khối lượng các ion.
.png)
= 0,01.96 + 0,01.60 + 0,005.137 + 0,015.207
= 5,35 gam
VI.37.
.png)
.png) : không phản ứng
: không phản ứng
.png)
(hoặc nhận xét ngay: .png) = tổng số mol muối)
= tổng số mol muối)
.png) = 0,06 + 0,015 = 0,075 mol
= 0,06 + 0,015 = 0,075 mol
.png) = 0,075.22,4 = 1,68 lít
= 0,075.22,4 = 1,68 lít
.png)
VI.38. Gọi .png) là khối lượng nguyên tử trung bình của 2 kim loại
là khối lượng nguyên tử trung bình của 2 kim loại .png)
.png)
Hai kim loại kiềm ở hai chu kì kế tiếp là: Li (M = 6,9) và Na (M = 23).
VI.39. KCl không bị nhiệt phân
.png)
Chú ý rằng trong 152 gam bã rắn có cả .png) .
.
.png)
VI.40.
.png)
Chất rắn: NaCl + NaOH = 15,7 gam
VI.41.
.png)
Khối lượng .png) ban đầu = 168,2 +
ban đầu = 168,2 + .png) = 168,2 + 76,8 = 245 g
= 168,2 + 76,8 = 245 g
Hiệu suất phản ứng = .png) .100% = 80%
.100% = 80%
VI.47.
Số p = .png) = 20 = số e
= 20 = số e
R: .png)
⇒ R ở chu kì 4, nhóm IIA.
VI.48. Vì .png) nên trong dung dịch các ion
nên trong dung dịch các ion .png) tồn tại ở cả hai dạng muối bicacbonat và clorua. Nước cứng toàn phần.
tồn tại ở cả hai dạng muối bicacbonat và clorua. Nước cứng toàn phần.
VI.49. .png)
Các phản ứng khi cho dung dịch .png) vào dung dịch A:
vào dung dịch A:
.png)
Trong dung dịch A, gọi số mol .png) = a mol
= a mol
Dung dịch A trung hòa điện nên:
a + 0,05.2 = 0,2.1
a = 0,1 mol
.png)
.png) = 0,05.96 +0,2.18 + 0,1.62 = 14,6 gam
= 0,05.96 +0,2.18 + 0,1.62 = 14,6 gam
VI.50. .png) = 0,4.1 = 0,4 mol
= 0,4.1 = 0,4 mol
.png)
.png) = 0,4.0,01 = 0,004 (mol)
= 0,4.0,01 = 0,004 (mol)
.png)
(.png) dư nên chỉ tạo ion
dư nên chỉ tạo ion .png) )
)
→ Phản ứng tạo muối trung tính, nhưng chỉ có .png) .
.
Và tính theo .png) :
:
.png)
VI.51. pH = 14 → pOH = 14 - 14 = 0
→ .png) = 1M
= 1M
.png)
.png) = 0,5.0,1 = 0,05 mol
= 0,5.0,1 = 0,05 mol
.png) = 3,94 : 197 = 0,02 mol
= 3,94 : 197 = 0,02 mol
* Nhận xét: Vì .png) ⇒ xét 2 trường hợp:
⇒ xét 2 trường hợp:
• Trường hợp 1: (.png) còn dư sau phản ứng)
còn dư sau phản ứng)
.png)
.png) = 0,02.22,4 = 0,448 lít
= 0,02.22,4 = 0,448 lít
• Trường hợp 2: (xảy ra cả hai phản ứng)
.png)
.png) = 0,02 + 0,06 = 0,08
= 0,02 + 0,06 = 0,08
.png) = 0,08.22,4 = 1,792 lít
= 0,08.22,4 = 1,792 lít
VI.52.
.png)
.png) dung dịch sẽ có 0,06 mol
dung dịch sẽ có 0,06 mol .png)
.png)
V = .png) = 0,06 lít = 60 ml
= 0,06 lít = 60 ml
VI.53.
.png)
Vì dư .png) nên có phản ứng tiếp theo.
nên có phản ứng tiếp theo.
.png)
Lấy (1) + (2) ta được phương trình hóa học sau:
.png)
.png) = 0,0075.197 = 1,4775 gam
= 0,0075.197 = 1,4775 gam
VI.54.
Đặt .png) là nguyên tử lượng trung bình của hai kim loại:
là nguyên tử lượng trung bình của hai kim loại:
.png) = 6,72 : 22,4 = 0,3 mol
= 6,72 : 22,4 = 0,3 mol
.png)
.png)
⇒ hai kim loại là Mg và Ca.
VI.55.
.png) = 1 mol;
= 1 mol; .png) = 1,5 mol
= 1,5 mol
.png)
⇒ xảy ra 2 phản ứng
.png)
.png)
VI.56.
.png) = 0,09 mol
= 0,09 mol
.png)
Ta có: a + b = 0,09
100a + 84b = 8,2
a = 0,04 = .png) , m = 4 gam
, m = 4 gam
b = 0,05 = .png) , m = 4,2 gam
, m = 4,2 gam
VI.57. Theo giả thiết cho thấy .png) đã tác dụng với
đã tác dụng với .png) theo 2 phản ứng:
theo 2 phản ứng:
.png)
Tổng số mol .png) = 0,1 + 0,1 = 0,2 mol
= 0,1 + 0,1 = 0,2 mol
.png) = 0,2.22,4 = 4,48 lít
= 0,2.22,4 = 4,48 lít
VI.58.
.png) = 0,1 mol
= 0,1 mol
.png) = 0,05 mol;
= 0,05 mol; .png) = 0,2 mol
= 0,2 mol
Tổng số mol .png) = 2.0,05 + 0,2 = 0,3 mol và 0,05 mol
= 2.0,05 + 0,2 = 0,3 mol và 0,05 mol .png) .
.
.png)
Vậy .png) = 0,05.100 = 5 gam
= 0,05.100 = 5 gam
VI.59. .png) = 6,96 : 87 = 0,08 mol
= 6,96 : 87 = 0,08 mol
.png)
(M + 71).0,08 = 7,6
M = 24; M là Mg
VI.60.
* Gọi muối cacbonat của kim loại kiềm là .png) và muối cacbonat của kim loại kiềm thổ là
và muối cacbonat của kim loại kiềm thổ là .png) .
.
.png)
* Nhận xét: .png) = 1,68 : 22,4 = 0,075 mol
= 1,68 : 22,4 = 0,075 mol
.png) = 2.0,075 = 0,15 mol
= 2.0,075 = 0,15 mol
.png)
= 5 + 0,15.36,5 – (44 + 18).0,075 = 5,825 gam
VI.61.
.png)
.png) = 0,2(84 + 100) = 36,8 gam
= 0,2(84 + 100) = 36,8 gam
.png) =
= .png) .100% = 92%
.100% = 92%
VI.62.
.png)
Vì .png) ⇒ xảy ra 2 phản ứng:
⇒ xảy ra 2 phản ứng:
.png)
Ta có :
.png)
.png) = a + b = 0,12 + 0,04 = 0,16
= a + b = 0,12 + 0,04 = 0,16
.png)
VI.63.
.png) = 3,36 : 22,4 = 0,15 mol
= 3,36 : 22,4 = 0,15 mol
.png) = 0,15.71 = 10,65 g
= 0,15.71 = 10,65 g
.png)
.png) = 15,05 – 10,65 = 4,4 g
= 15,05 – 10,65 = 4,4 g
VI.64. Kim loại kiềm: M
.png)
Kim loại kiềm thổ: X
.png)
Nhận xét: số mol .png) = 2.
= 2..png) = 2.0,12 = 0,24 mol
= 2.0,12 = 0,24 mol
.png)
.png) = 0,12 : 0,5 = 0,24 l = 240 ml
= 0,12 : 0,5 = 0,24 l = 240 ml
VI.71.
.png)
.png) không tan trong
không tan trong .png) .
.
.png)
.png) tan được trong
tan được trong .png) do tạo phức chất.
do tạo phức chất.
.png)
nên kết tủa chỉ có .png) .
.
.png)
* CO không khử được .png)
Vậy rắn C là .png) .
.
VI.72.
.png)
.png) bị hòa tan trong HCl (dư):
bị hòa tan trong HCl (dư):
.png)
VI.76.
* Hòa tan từng chất vào nước:
- Chất tan, tạo thành dụng dịch trong suốt là .png) .
.
.png)
* Dùng dung dịch NaOH để nhận biết .png) (tan trong dd NaOH) và MgO (không tan trong dd NaOH).
(tan trong dd NaOH) và MgO (không tan trong dd NaOH).
VI.77. Chú ý:
.png)
.png) không tan khi cho dư
không tan khi cho dư .png) .
.
.png)
.png) tan khi cho dư
tan khi cho dư .png) do tạo phức tan
do tạo phức tan
.png)
VI.78. * Dùng .png) để nhận biết
để nhận biết
- Tan trong nước, không có khí thoát ra là .png)
- Tan trong nước, có khí thoát ra là Na
- Không tan trong nước là Al, .png) , MgO
, MgO
* Dùng dd NaOH thu được để nhận ra 3 chất còn lại.
- Tan trong dd NaOH, không có khí thoát ra là .png)
- Tan trong dung dịch NaOH và có khí thoát ra là Al
- Không tan trong dd NaOH là MgO.
VI.80. Chỉ có các phản ứng:
.png)
Các oxit .png) , MgO không tác dụng với CO,
, MgO không tác dụng với CO, .png) .
.
Trong Y có Fe, Cu, .png) , MgO.
, MgO.
Chọn C.
VI.81.
.png)
Khối lượng chất rắn tăng bằng .png) phản ứng:
phản ứng:
.png) = 4,26 : 71 = 0,06 mol
= 4,26 : 71 = 0,06 mol
.png) =
= .png) .0,06 = 0,04 mol
.0,06 = 0,04 mol
→ .png) = 1,08 gam
= 1,08 gam
VI.82. .png) = 2.0,2 = 0,4 mol
= 2.0,2 = 0,4 mol
.png) = 6,72 : 22,4 = 0,3 mol
= 6,72 : 22,4 = 0,3 mol
.png)
VI.86.
.png)
Gọi số mol .png) : 2a mol
: 2a mol
NO: a mol
.png) : 2a mol
: 2a mol
* Sơ đồ cho và nhận electron
.png)
* Ta có: 39a = 1,56
a = 0,04 (mol)
.png) = 5a.22,4 = 5.0,04.22,4 = 4,48 lít
= 5a.22,4 = 5.0,04.22,4 = 4,48 lít
VI.87. * Các phản ứng có thể xảy ra
.png)
* Vì còn kết tủa .png) (Y), nên trong dung dịch X không thể có
(Y), nên trong dung dịch X không thể có .png) .
.
VI.88. * Nhận xét: Vì phản ứng hoàn toàn mà hỗn hợp sau phản ứng tác dụng với NaOH có khí thoát ra, suy ra Al còn dư, .png) hết. Nhân đôi thể tích khí cho cả hỗn hợp.
hết. Nhân đôi thể tích khí cho cả hỗn hợp.
* Đặt số mol .png) là a mol,
là a mol, .png) dư là b mol.
dư là b mol.
.png)
* Hỗn hợp sau phản ứng + NaOH: chỉ có .png) và Al phản ứng trong đó chỉ có phản ứng của Al giải phóng khí.
và Al phản ứng trong đó chỉ có phản ứng của Al giải phóng khí.
.png)
* Hỗn hợp sau phản ứng + HCl: chỉ có Fe, Al → khí, còn .png) phản ứng không tạo ra khí.
phản ứng không tạo ra khí.
.png)
.png)
* Khối lượng hỗn hợp ban đầu:
.png)
m = 0,6.232 +( .png) .0,6 + 0,4).27 = 193,2 g
.0,6 + 0,4).27 = 193,2 g
VI.89. Chọn 1 mol Al cho các phản ứng:
.png)
VI.90.
* m gam hỗn hợp A + .png) dư → khí + rắn C (Al còn dư)
dư → khí + rắn C (Al còn dư)
Gọi số mol Ba là a mol (trong m gam hỗn hợp).
* TN1: hh + .png) dư?
dư?
.png)
Ta có: a + 3a = .png) = 0,06
= 0,06
a = 0,015 = .png)
.png) = 0,015.137 = 2,055 gam
= 0,015.137 = 2,055 gam
* TN2: hh + dd .png) dư ⇒ Al hết: 2b mol
dư ⇒ Al hết: 2b mol
.png)
Ta có: 2a + 3b = .png) = 0.93
= 0.93
b = 0,3 = .png) (trong m gam hỗn hợp)
(trong m gam hỗn hợp)
.png) = 0,3.27 = 8,1 gam
= 0,3.27 = 8,1 gam
