CHƯƠNG BẢY: SẮT VÀ MỘT SỐ KIM LOẠI QUAN TRỌNG
SẮT
I. Cấu tạo nguyên tử và tính chất vật lí
* Fe (Z = 26) theo mức năng lượng
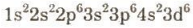
⇒ Cấu hình electron
.png) hay
hay .png)
Sắt thuộc chu kì 4, nhóm VIII B.
* Sắt là kim loại màu trắng hơi xám, có khối lượng riêng lớn (D = 7,9 .png) ), nóng chảy ở 1540°C, dẫn điện, dẫn nhiệt tốt. Sắt có tính nhiễm từ.
), nóng chảy ở 1540°C, dẫn điện, dẫn nhiệt tốt. Sắt có tính nhiễm từ.
(Chú ý: khi ở dạng bột, bột sắt có màu đen)
II. Tính chất hóa học
* Trong các phản ứng hóa học, nguyên tử Fe có thể nhường 2 hoặc 3 electron, tạo ion .png) .
.
Do vậy sắt có hai hóa trị là II và III.
1. Tác dụng với oxi và phi kim khác
.png)
2. Tác dụng với axit
+ Với HCl, .png) loãng, RCOOH →
loãng, RCOOH → .png) + Muối sắt (II)
+ Muối sắt (II)
Thí dụ:
.png)
+ Với .png) đặc, nóng → muối sắt (III) + khí
đặc, nóng → muối sắt (III) + khí
Thí dụ:
.png)
Chú ý: Fe không tác dụng với .png) đặc và nguội.
đặc và nguội.
.png)
3. Tác dụng với dung dịch muối của kim loại yếu hơn
Thí dụ
.png)
Chú ý: .png)
Nếu dư .png) , phản ứng tiếp theo:
, phản ứng tiếp theo:
.png)
4. Tác dụng với nước ở nhiệt độ cao
.png)
